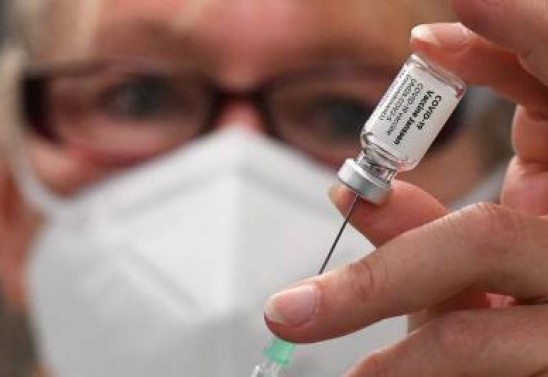
A Agência Nacional de Vigilância Sanitária (Anvisa) informou que recebeu o pedido para avaliar a inclusão de dose de reforço do imunizante Janssen na bula. A vacina contra a covid-19 tem esquema primário de dose única. A proposta de reforço deve manter ou elevar a imunização.
O pedido da farmacêutica prevê a indicação da Janssen em duas situações: como reforço homólogo (mesma vacina): destinado a pessoas que foram imunizadas com a Janssen; e o heterólogo (diferente) imunizante de tecnologia mRNA. Atualmente a única vacina de mRNA aprovada no Brasil é a Pfizer.
A Anvisa afirmou que vai analisar a solicitação da farmacêutica após a análise de dados e estudos desenvolvidos pela empresa. As possíveis condições de uso, indicações e intervalos serão definidos pela Agência a partir das informações e evidências científicas disponíveis.
As informações são de responsabilidade da empresa e devem demonstrar o benefício da dose de reforço em relação a segurança e eficácia. O pedido foi protocolado na noite de sexta-feira (19/11) e prazo de análise é de até 30 dias, conforme regras adotadas dentro da autorização de uso emergencial.